
在由铜片、锌片和200 mL稀H2SO4组成的原电池中,若锌片只发生电化学腐蚀,当在铜片上放出3.36 L(标准状况)的H2时,H2SO4恰好用完,则产生这些气体消耗的Zn为__\_g,在导线上有__mol电子通过,原稀H2SO4的物质的量浓度是_______ mol/L。
下列说法正确的是
[ ]
A.1molCl2与足量Fe反应,转移电子的物质的量为2mol B.工业火法炼铜:Cu2S+O2=2Cu+SO2每生成2mol铜,反应共转移2mol 电子 C.称取25g CuSO4 5H2O固体溶于75g水中,所得溶液中溶质的质量分数为25% D.元素周期表中第Ⅷ族元素种类在各族中最多
5H2O固体溶于75g水中,所得溶液中溶质的质量分数为25% D.元素周期表中第Ⅷ族元素种类在各族中最多
下列地形区与其特点组合正确的一组是
[ ]
A、内蒙古平原——崎岖不平B、云贵高原——雪山连绵C、四川盆地——地形平坦D、东北平原——黑土广布
我国水能蕴藏量最丰富的地区
[ ]
A、地势第一和第二级阶梯交界地带B、地势第二、三级阶梯交界地带C、青藏高原、东南丘陵D、各大河流的中下游地带
如图为某电解装置,均用铂作电极,测得电流强度I=5.5A,通电7.3h后,在丙容器中使100g14.0%的硫酸钠溶液电解得到气体总体积(标准状况下)为16.8L,没有析出晶体。
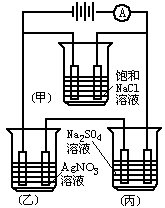
请回答:(1)通电7.3h后,丙容器溶液中溶质的质量分数_______。(溶剂挥发忽略不计,必须写出相关化学方程式及计算过程)(2)乙容器中,阴极得到银的质量为____。(3)甲容器放入50LNaC1溶液(设电解后溶液的体积不变)。电解后溶液的pH是多少?_______(已知1mol电子所带的电量为96500C)(必须写出相关化学方程式及计算过程)