氢化物、火焰、石墨炉原子吸收: 1.为什么砷、锑、铋,锡,,等用氢化物发生器测定比较好 2.对于上述元素用氢化物和石墨炉测定哪个方法的DL更好? 3.火焰温度2300度左右,而用氢化物测定时一般在800-900度,按理说的话火焰的原子化也可以啊,为什么氢化物的DL更好?
某主族元素R的最高正价与最低负化合价的代数和为4,由此可以判断()。
A.R一定是第四周期元素
B.R一定是ⅣA族元素
C.R的气态氢化物比同周期其他元素气态氢化物稳定
D.R气态氢化物的化学式为H2R
氢化物原子荧光光谱法测定食品中的砷和氢化物原子荧光光谱法测定食品中的汞其原理完全相同
A、对
B、错
能以金属氢化物的形式吸收氢,加热后又能释放氢的金属称为()。
A、氢化合金
B、储氢合金
C、氢脆
D、氢化物
原子荧光光度计由四个部分组成()。
A、光源
B、氢化物发生(断续流动和自动进样、氢化物反应系统)
C、原子化系统
D、检测系统
下表是元素周期表的一部分:
周期 族
IA
IIA
IIIA
IVA
V A
VIA
VIIA
2
②
③
④
⑤
⑥
3
⑦
⑧
⑨
⑩
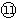
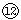
(1)表中元素⑩的氢化物的化学式为_____,此氢化物的还原性比元素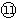 的氢化物的还原性____稳定性 (填强或弱)(2)某元素的原子结构示意图为:
的氢化物的还原性____稳定性 (填强或弱)(2)某元素的原子结构示意图为: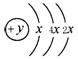 ,在周期表位于 。该氢化物沸点比甲烷 (填高或低)。(3)用电子式表示
,在周期表位于 。该氢化物沸点比甲烷 (填高或低)。(3)用电子式表示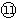 与⑧形成化合物形成过程: 。(4)写出⑦与⑨、⑨与
与⑧形成化合物形成过程: 。(4)写出⑦与⑨、⑨与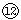 的最高价氧化物对应水化物反应的离子方程式:⑦与⑨: 、⑨与
的最高价氧化物对应水化物反应的离子方程式:⑦与⑨: 、⑨与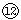 。
。
某元素R的最高价氧化物的分子式为,它的最低价气态氢化物中含氢12.5%(质量分数).该气态氢化物的相对分子质量为( ).
A、32
B、34
C、28
D、16
用氢化物原子荧光光谱法测铅,将铅变为挥发性的氢化物的是()。
A、锌粒加酸
B、硼氢化钠或硼氢化钾
C、氢氧化钠
D、金属钠加水
E、纯氢
用氢化物原子荧光光谱法测铅时,能将铅变为挥发性氢化物的是()
A、锌粒加酸
B、氢氧化钠
C、纯氢
D、硼氢化钠或硼氢化钾
E、金属钠加水
A锌粒加酸
B硼氢化钠或硼氢化钾
C氢氧化钠
D金属钠加水
E纯氢
《化妆品卫生规范》中规定的砷的测定方法是
A、分光光度法
B、氢化物原子吸收法
C、氢化物原子荧光光度法
D、二乙氨基二硫代甲酸银分光光度法
E、砷斑法
氢化物发生器是一种使被分析元素与还原剂(通常为硼氢化钠)发生化学反应,产生挥发性氢化物,然后通到石英池加热还原成激发态原子的技术
A、对
B、错
采用氢化物-原子荧光法可以分别测定食品中As(Ⅴ)和As(Ⅲ)等不同的价态形式,这是何种因素决定的
A、在不同介质中的氢化反应速度
B、温度的影响
C、氢化物浓度的影响
D、激发能量
E、吸收波长
“类推”是常用的学习方法,但有时会产生错误结论。下列类推的结论中,正确的是( )
AⅣA族元素氢化物沸点顺序是GeH4>SiH4>CH4;则ⅤA族元素氢化物沸点顺序也是AsH3>PH3>NH3
B第二周期元素氢化物稳定性顺序是HF>H2O>NH3;则第三周期元素氢化物稳定性顺序也是HCl>H2S>PH3
C晶体中有阴离子,必有阳离子;则晶体中有阳离子,也必有阴离子
D干冰(CO2)是分子晶体;则二氧化硫(SO2)也是分子晶体
采用氢化物-原子荧光法可以分别测定食品中As(V)和As(Ⅲ)等不同的价态形式,这是下列哪种因素决定的()
A、在不同介质中的氢化反应速度
B、温度的影响
C、氢化物浓度的影响
D、激发能量
E、吸收波长
(15分)(注意:在试题卷上作答无效)
已知周期表中,元素Q、R、W、Y与元素X相邻。Y的最高化合价氧化物的水化物是强酸。回答下列问题:
(1)W与Q可以形成一种高温结构陶瓷材料。W的氯化物分子呈正四面体结构,W的氧化物的晶体类型是;
(2)Q的具有相同化合价且可以相互转变的氧化物是;
(3)R和Y形成的二元化合物中,R呈现最高化合价的化合物的化学式是;
(4)这5个元素的氢化物分子中,①立体结构类型相同的氢化物的沸点从高到低排列次序是(填化学式),其原因是
;
②电子总数相同的氢化物的化学式和立体结构分别是
;
(5)W和Q所形成的结构陶瓷材料的一种合成方法如下:W的氯化物与Q的氢化物加热反应,生成化合物W(QH2)4和HCL气体;W(QH2)4在高温下分解生成Q的氢化物和该陶瓷材料。上述相关反应的化学方程式(各物质用化学式表示)是。
近年来发展了一种低温原子化法—气相氢化物原子化法,用以测定As、Sb、Bi、Ge、Sn、Se、Te等元素。下列使之生成熔点、沸点低的共价分子型氢化物的还原剂是()
A、H2
B、Zn
C、Na2S2O3
D、NaBH4
近年来,一种新型简便的储氢方法应运而生,即利用储氢合金(金属氢化物)来储存氢气。研究证明,某些金属具有很强的捕捉氢的能力,在一定的温度和压力条件下,这些金属能够大量“吸收”氢气,反应生成金属氢化物,同时放出热量。其后,将这些金属氢化物加热,它们又会分解,将储存在其中的氢释放出来。这些会“吸收”氢气的金属,称为储氢合金。则下列说法中不正确的是()
A、氢气在储存过程中主要发生了物理变化
B、氢能源是未来理想的能源
C、氢气在储存过程中化学能部分转化为内能
D、氢气在储存过程中主要发生了化学变化
下列说法正确的是()。
A.稀有气体单质由原子组成,所以它们在固态时形成原子晶体
B.常温下是气体的物质,在固态时都是分子晶体,所以熔、沸点都较低
C.同族元素的共价型氢化物,其相对分子量愈大,分子间相互作用力愈小
D.同族元素的共价型氢化物,其相对分子量愈大,分子间相互作用力愈大